Atrofimizdagi tabiat hodisalari va jarayonlari ancha murakkab. Ularning aniq jismoniy tavsifi uchun mashaqqatli matematik apparatdan foydalanish va ko'plab muhim omillarni hisobga olish kerak. Ushbu muammoning oldini olish uchun fizikada ba'zi soddalashtirilgan modellar qo'llaniladi, ular jarayonning matematik tahlilini sezilarli darajada osonlashtiradi, lekin uni tavsiflashning to'g'riligiga amalda ta'sir qilmaydi. Ulardan biri ideal gaz modelidir. Keling, buni maqolada batafsil ko'rib chiqaylik.
Ideal gaz tushunchasi
Ideal gaz - bir-biri bilan o'zaro ta'sir qilmaydigan moddiy nuqtalardan tashkil topgan moddaning agregatsiya holati. Keling, bu taʼrifni batafsilroq tushuntiramiz.
Birinchidan, biz ideal gazni tashkil etuvchi jismlar sifatida moddiy nuqtalar haqida bormoqda. Bu shuni anglatadiki, uning molekulalari va atomlari o'lchamga ega emas, balki ma'lum bir massaga ega. Bu jasurpast bosim va yuqori haroratdagi barcha real gazlarda molekulalar orasidagi masofa ularning chiziqli oʻlchamlaridan ancha katta ekanligini hisobga olgan holda taxminiy hisoblash mumkin.
Ikkinchidan, ideal gazdagi molekulalar bir-biri bilan oʻzaro taʼsir qilmasligi kerak. Aslida, bunday o'zaro ta'sirlar doimo mavjud. Shunday qilib, hatto asil gazlarning atomlari ham dipol-dipol tortishish xususiyatiga ega. Boshqacha qilib aytganda, van der Waals o'zaro ta'siri mavjud. Biroq, molekulalarning aylanish va translatsion harakatining kinetik energiyasi bilan solishtirganda, bu o'zaro ta'sirlar shunchalik kichikki, ular gazlarning xususiyatlariga ta'sir qilmaydi. Shuning uchun amaliy masalalarni yechishda ularni hisobga olish mumkin emas.
Shuni ta'kidlash kerakki, zichligi past va harorati yuqori bo'lgan barcha gazlarni ideal deb hisoblash mumkin emas. Van der Vaals o'zaro ta'siridan tashqari, boshqa kuchliroq bog'lanish turlari mavjud, masalan, H2O molekulalari orasidagi vodorod aloqalari, bu gaz ideallik shartlarini qo'pol ravishda buzilishiga olib keladi. Shuning uchun suv bug'i ideal gaz emas, balki havo idealdir.
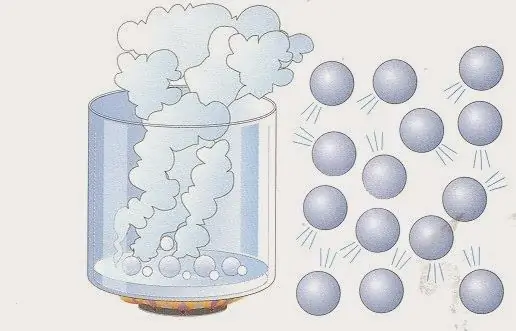
Ideal gazning fizik modeli
Ushbu modelni quyidagicha ifodalash mumkin: gaz tizimida N zarracha bor deylik. Bular turli xil kimyoviy moddalar va elementlarning atomlari va molekulalari bo'lishi mumkin. N zarrachalar soni koʻp, shuning uchun uni tasvirlash uchun odatda “mol” birligi qoʻllaniladi (1 mol Avogadro soniga toʻgʻri keladi). Ularning barchasi ma'lum hajmda harakat qiladi V. Zarrachalar harakatitartibsiz va bir-biridan mustaqil. Ularning har biri ma'lum v tezligiga ega va to'g'ri yo'l bo'ylab harakatlanadi.
Nazariy jihatdan zarralar orasidagi toʻqnashuv ehtimoli deyarli nolga teng, chunki ularning oʻlchamlari zarralar orasidagi masofalarga nisbatan kichik. Biroq, agar bunday to'qnashuv sodir bo'lsa, unda u mutlaqo elastikdir. Ikkinchi holda, zarrachalarning umumiy impulsi va ularning kinetik energiyasi saqlanadi.
Ideal gazlarning ko'rib chiqilgan modeli juda ko'p sonli elementlarga ega klassik tizimdir. Shuning uchun undagi zarrachalarning tezligi va energiyasi Maksvell-Boltzmanning statistik taqsimotiga bo'ysunadi. Ba'zi zarralar past tezlikka ega, boshqalari esa yuqori tezlikka ega. Bunday holda, ma'lum bir tor tezlik chegarasi mavjud bo'lib, unda ushbu miqdorning eng mumkin bo'lgan qiymatlari yotadi. Azot molekulalarining tezlik taqsimoti quyida sxematik tarzda ko'rsatilgan.
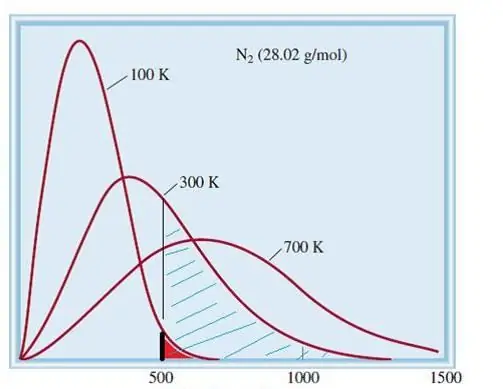
Gazlarning kinetik nazariyasi
Yuqorida tavsiflangan ideal gazlar modeli gazlarning xossalarini yagona tarzda aniqlaydi. Bu model birinchi marta 1738 yilda Daniel Bernulli tomonidan taklif qilingan.

Keyinchalik u Avgust Kroenig, Rudolf Klauzius, Mixail Lomonosov, Jeyms Maksvell, Lyudvig Boltsmann, Marian Smoluchovski va boshqa olimlar tomonidan hozirgi holatga keltirildi.
Suyuq moddalarning kinetik nazariyasi, uning asosida ideal gaz modeli tuziladi, tizimning mikroskopik xatti-harakatlariga asoslangan ikkita muhim makroskopik xususiyatlarini tushuntiradi:
- Gazlardagi bosim zarrachalarning idish devorlari bilan toʻqnashishi natijasidir.
- Tizimdagi harorat molekulalar va atomlarning doimiy harakatining namoyon boʻlishi natijasidir.
Kinetik nazariyaning ikkala xulosasini ham kengaytiramiz.
Gaz bosimi
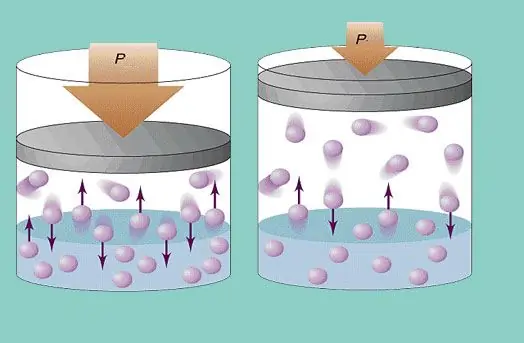
Ideal gaz modeli tizimdagi zarrachalarning doimiy xaotik harakatini va ularning tomir devorlari bilan doimiy toʻqnashuvini nazarda tutadi. Har bir bunday to'qnashuv mutlaqo elastik hisoblanadi. Zarracha massasi kichik (≈10-27-10-25 kg). Shuning uchun u to'qnashuvda katta bosim hosil qila olmaydi. Shunga qaramay, zarrachalar soni va shuning uchun to'qnashuvlar soni juda katta (≈1023). Bundan tashqari, elementlarning o'rtacha kvadrat tezligi xona haroratida soniyasiga bir necha yuz metrni tashkil qiladi. Bularning barchasi tomir devorlariga sezilarli bosimning paydo bo'lishiga olib keladi. Uni quyidagi formula yordamida hisoblash mumkin:
P=Nmvcp2 / (3V), bu erda vcp - o'rtacha kvadrat tezlik, m - zarracha massasi.
Mutlaq harorat
Ideal gaz modeliga ko'ra, harorat o'rganilayotgan tizimdagi molekula yoki atomning o'rtacha kinetik energiyasi bilan yagona aniqlanadi. Siz ideal gaz uchun kinetik energiya va mutlaq haroratni bog'laydigan quyidagi ifodani yozishingiz mumkin:
mvcp2 / 2=3 / 2kB T.
Bu yerda kB - Boltsman doimiysi. Ushbu tenglikdan biz olamiz:
T=m vcp2 / (3kB).
Universal holat tenglamasi
Agar mutlaq bosim P va mutlaq harorat T uchun yuqoridagi ifodalarni birlashtirsak, quyidagi tenglikni yozishimiz mumkin:
PV=nRT.
Bu yerda n-moddaning moldagi miqdori, R-D. I. Mendeleyev kiritgan gaz konstantasi. Bu ifoda ideal gazlar nazariyasidagi eng muhim tenglama hisoblanadi, chunki u uchta termodinamik parametrni (V, P, T) birlashtiradi va gaz tizimining kimyoviy xususiyatlariga bog'liq emas.

Umumjahon tenglama birinchi marta 19-asrda frantsuz fizigi Emil Klapeyron tomonidan eksperimental ravishda olingan va keyin rus kimyogari Mendeleyev tomonidan zamonaviy ko'rinishga keltirildi, shuning uchun ham u hozirda ushbu olimlarning nomi bilan ataladi.






