Gazning issiqlik sig'imi - bu jism bir daraja qizdirilganda o'zlashtiradigan energiya miqdori. Keling, ushbu jismoniy miqdorning asosiy xususiyatlarini tahlil qilaylik.

Tanriflar
Gazning solishtirma issiqligi ma'lum bir moddaning birlik massasidir. Uning o'lchov birliklari J/(kg·K). Agregat holatini o'zgartirish jarayonida organizm tomonidan so'rilgan issiqlik miqdori nafaqat boshlang'ich va yakuniy holat, balki o'tish usuli bilan ham bog'liq.

Boʻlim
Gazlarning issiqlik sig'imi doimiy hajmda (Cv), doimiy bosimda (Cr) aniqlangan qiymatga bo'linadi.
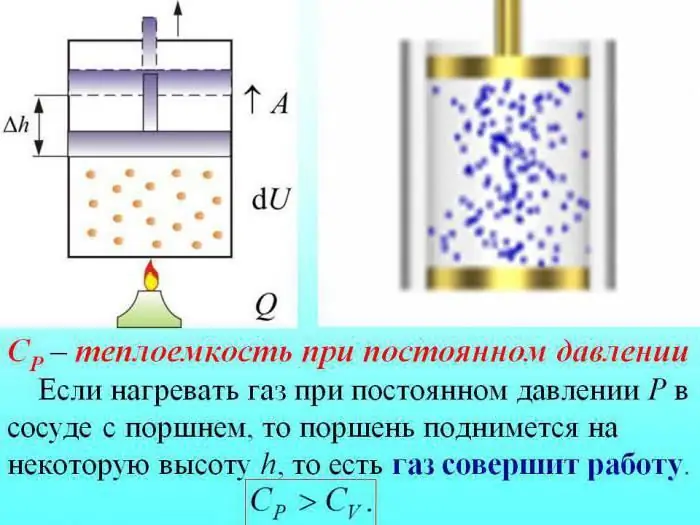
Bosim oʻzgarmagan holda qizdirilganda issiqlikning bir qismi gazni kengaytirish ishini ishlab chiqarishga, energiyaning bir qismi esa ichki energiyani oshirishga sarflanadi.
Oʻzgarmas bosimdagi gazlarning issiqlik sigʻimi ichki energiyani oshirishga sarflangan issiqlik miqdori bilan aniqlanadi.
Gaz holati: xususiyatlari, tavsifi
Ideal gazning issiqlik sig`imi Sp-Sv=R ekanligini hisobga olgan holda aniqlanadi. Oxirgi miqdor universal gaz doimiysi deb ataladi. Uning qiymati 8,314 J/(mol K) ga to‘g‘ri keladi.
Issiqlik sig`imining nazariy hisob-kitoblarini amalga oshirishda, masalan, harorat bilan bog`liqlikni tavsiflashda faqat termodinamik usullardan foydalanishning o`zi kifoya emas, o`zingizni statik fizika elementlari bilan qurollantirish muhimdir.
Gazlarning issiqlik sig'imi ba'zi molekulalarning tarjima harakati energiyasining o'rtacha qiymatini hisoblashni o'z ichiga oladi. Bunday harakat molekulaning aylanish va translatsiya harakati, shuningdek, atomlarning ichki tebranishlaridan iborat.
Statik fizikada aylanma va translatsiya harakati erkinligining har bir darajasi uchun universal gaz konstantasining yarmiga teng boʻlgan gaz miqdori borligi haqidagi maʼlumotlar mavjud.

Qiziqarli faktlar
Monaatomik gazning zarrasi uchta translatsion erkinlik darajasiga ega deb hisoblanadi, shuning uchun gazning solishtirma issiqligi uchta tarjima, ikkita aylanish va bir tebranish erkinlik darajasiga ega. Ularning bir xil taqsimlanish qonuni doimiy hajmdagi solishtirma issiqlikni R ga tenglashtirishga olib keladi.
Tajribalar davomida ikki atomli gazning issiqlik sig`imi R qiymatiga mos kelishi aniqlandi. Nazariya va amaliyot o`rtasidagi bunday nomuvofiqlik ideal gazning issiqlik sig`imi kvant bilan bog`liqligi bilan izohlanadi. ta'sirlar, shuning uchun hisob-kitoblarni amalga oshirishda kvantga asoslangan statistik ma'lumotlardan foydalanish muhimdirmexanika.
Kvant mexanikasi asoslariga asoslanib, tebranuvchi yoki aylanuvchi zarrachalar tizimi, jumladan, gaz molekulalari faqat ba'zi diskret energiya qiymatlariga ega.
Agar tizimdagi issiqlik harakatining energiyasi ma'lum chastotali tebranishlarni qo'zg'atish uchun etarli bo'lmasa, bunday harakatlar tizimning umumiy issiqlik sig'imiga hissa qo'shmaydi.
Natijada ma'lum bir erkinlik darajasi "muzlatib qoladi", unga teng bo'lish qonunini qo'llash mumkin emas.
Gazlarning issiqlik sig'imi butun termodinamik tizimning ishlashi bog'liq bo'lgan holatning muhim xarakteristikasidir.
Tebranish yoki aylanish erkinlik darajasiga teng boʻlinish qonunini qoʻllash mumkin boʻlgan harorat kvant nazariyasi bilan tavsiflanadi, Plank doimiysini Boltsman doimiysi bilan bogʻlaydi.

Diatomik gazlar
Bunday gazlarning aylanish energiya darajalari orasidagi bo'shliqlar oz sonli darajadir. Istisno vodorod bo'lib, unda harorat qiymati yuzlab darajalar bilan belgilanadi.
Shuning uchun ham gazning doimiy bosimdagi issiqlik sig`imini bir xil taqsimlanish qonuni bilan tasvirlash qiyin. Kvant statistikasida issiqlik sig'imini aniqlashda uning tebranish qismi, harorat pasayganda, tez pasayib, nolga yetishi hisobga olinadi.
Bu hodisa xona haroratida issiqlik sigʻimining tebranish qismi deyarli yoʻqligini tushuntiradi.ikki atomli gaz, u doimiy R ga mos keladi.
Past harorat ko'rsatkichlari holatida doimiy hajmdagi gazning issiqlik sig'imi kvant statistikasi yordamida aniqlanadi. Termodinamikaning uchinchi qonuni deb ataladigan Nernst printsipi mavjud. Uning formulasidan kelib chiqqan holda, gazning molyar issiqlik sig'imi haroratning pasayishi bilan kamayadi va nolga intiladi.

Qattiq jismlarning xususiyatlari
Agar gazlar aralashmasining issiqlik sig`imini kvant statistikasi yordamida tushuntirish mumkin bo`lsa, u holda agregatsiyaning qattiq holati uchun issiqlik harakati muvozanat holatiga yaqin zarrachalarning ozgina tebranishlari bilan tavsiflanadi.
Har bir atom uchta tebranish erkinlik darajasiga ega, shuning uchun teng taqsimlanish qonuniga muvofiq, qattiq jismning molyar issiqlik sig'imi 3nR, n esa molekuladagi atomlar soni bilan hisoblanishi mumkin.
Amalda bu raqam qattiq jismning issiqlik sigʻimi yuqori haroratlarda moyil boʻladigan chegaradir.
Ba'zi elementlar, jumladan, metallar uchun oddiy haroratlarda maksimal qiymatga erishish mumkin. n=1 uchun Dyulong va Petit qonuni bajariladi, ammo murakkab moddalar uchun bunday chegaraga erishish ancha qiyin. Haqiqatda chegarani olish mumkin emasligi sababli, qattiq moddaning parchalanishi yoki erishi sodir bo'ladi.
Kvant nazariyasi tarixi
Kvant nazariyasining asoschilari XX asr boshlarida Eynshteyn va Debaydir. U ma'lum birdagi atomlarning tebranish harakatlarini kvantlashga asoslangankristall. Past harorat ko'rsatkichlari bo'lsa, qattiq jismning issiqlik sig'imi kub shaklida olingan mutlaq qiymatga to'g'ridan-to'g'ri proportsional bo'lib chiqadi. Bu munosabat Debay qonuni deb ataladi. Past va yuqori harorat ko'rsatkichlarini farqlash imkonini beruvchi mezon sifatida ularni Debye harorati bilan taqqoslash olinadi.
Bu qiymat tanadagi atomning tebranish spektri bilan belgilanadi, shuning uchun u jiddiy ravishda uning kristall tuzilishining xususiyatlariga bog'liq.
QD bir necha yuz K ga ega qiymatdir, lekin, masalan, olmosda u ancha yuqori.
O'tkazuvchi elektronlar metallarning issiqlik sig'imiga katta hissa qo'shadi. Uni hisoblash uchun Fermi kvant statistikasidan foydalaniladi. Metall atomlari uchun elektron o'tkazuvchanlik mutlaq haroratga to'g'ridan-to'g'ri proportsionaldir. Bu ahamiyatsiz qiymat bo'lgani uchun u faqat mutlaq nolga moyil bo'lgan haroratlarda hisobga olinadi.
Issiqlik sig'imini aniqlash usullari
Asosiy tajriba usuli - kaloriyametriya. Issiqlik sig'imini nazariy hisoblash uchun statistik termodinamikadan foydalaniladi. Bu ideal gaz uchun ham, kristall jismlar uchun ham amal qiladi, moddaning tuzilishi bo'yicha eksperimental ma'lumotlar asosida amalga oshiriladi.
Ideal gazning issiqlik sig'imini hisoblashning empirik usullari kimyoviy tuzilish g'oyasiga, atomlarning alohida guruhlarining Sr ga qo'shgan hissasiga asoslanadi.
Suyuqliklar uchun termodinamikdan foydalanishga asoslangan usullardan ham foydalaniladibug'lanish jarayonining entalpiyasi harorati hosilasi orqali ideal gazning issiqlik sig'imidan suyuqlikka o'tishga imkon beradigan davrlar.
Eritma holatida issiqlik sig'imini qo'shimcha funktsiya sifatida hisoblashga yo'l qo'yilmaydi, chunki eritmaning issiqlik sig'imining ortiqcha qiymati asosan muhim.
Uni baholash uchun bizga eritmalarning molekulyar-statistik nazariyasi kerak. Eng qiyini termodinamik tahlilda geterogen tizimlarning issiqlik sig'imini aniqlashdir.

Xulosa
Issiqlik sig'imini o'rganish kimyoviy reaktorlarda, shuningdek, boshqa kimyoviy ishlab chiqarish apparatlarida sodir bo'ladigan jarayonlarning energiya balansini hisoblash imkonini beradi. Bundan tashqari, bu qiymat sovutish suyuqliklarining optimal turlarini tanlash uchun zarur.
Hozirgi vaqtda moddalarning issiqlik sig'imini turli harorat oralig'ida - past qiymatlardan yuqori qiymatlargacha - eksperimental aniqlash moddaning termodinamik xususiyatlarini aniqlashning asosiy variantidir. Moddaning entropiyasi va entalpiyasini hisoblashda issiqlik sig'im integrallaridan foydalaniladi. Muayyan harorat oralig'ida kimyoviy reagentlarning issiqlik sig'imi haqidagi ma'lumotlar jarayonning issiqlik effektini hisoblash imkonini beradi. Eritmalarning issiqlik sig'imi haqidagi ma'lumotlar ularning termodinamik parametrlarini har qanday harorat qiymatlarida tahlil qilingan intervalda hisoblash imkonini beradi.
Masalan, suyuqlik potentsial energiya qiymatini o'zgartirish uchun issiqlikning bir qismini sarflashi bilan tavsiflanadi.reaksiyaga kirishuvchi molekulalar. Bu qiymat yechimlarni tavsiflash uchun ishlatiladigan "konfiguratsiya" issiqlik sig'imi deb ataladi.
Moddaning termodinamik xarakteristikalarini, uning yig’ilish holatini hisobga olmasdan turib, to’liq matematik hisob-kitoblarni amalga oshirish qiyin. Shuning uchun suyuqliklar, gazlar, qattiq jismlar uchun o'ziga xos issiqlik sig'imi kabi xususiyat qo'llaniladi, bu moddaning energiya parametrlarini tavsiflash imkonini beradi.






