Materiyaning gazsimon agregat holatining termodinamiği tizimlardagi termodinamik muvozanat va kvazistatik oʻtishlarni oʻrganuvchi fizikaning muhim boʻlimidir. Tizimlarning xatti-harakatlarini bashorat qilishga asoslangan asosiy model ideal gaz modelidir. Uning ishlatilishi bilan Mendeleyev-Klapeyron tenglamasi olingan. Buni maqolada ko'rib chiqing.
Ideal gaz
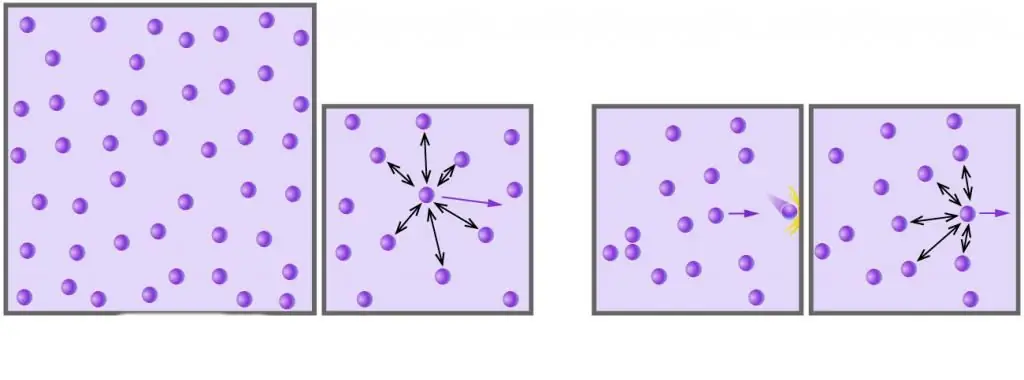
Ma'lumki, barcha haqiqiy gazlar molekula yoki atomlardan iborat bo'lib, ular orasidagi masofalar past bosimdagi o'lchamlariga nisbatan juda katta. Bundan tashqari, yuqori haroratlarda, mutlaq miqyosda, molekulalarning kinetik energiyasi zaif dipol-dipol o'zaro ta'siri bilan bog'liq bo'lgan potentsial energiyasidan oshadi (agar bu o'zaro ta'sirlardan tashqari, kimyoviy bog'lanishlarning boshqa turlari mavjud bo'lsa, masalan, ion yoki vodorod, keyin ular ichki tizim energiyasining potentsial komponentiga katta hissa qo'shadilar).
Shu sababliKo'pgina real gazlar uchun normaga yaqin sharoitda ularning ichki o'zaro ta'siri va zarracha o'lchamlarini e'tiborsiz qoldirish mumkin. Bu ikki asosiy taxmin ideal gaz modelini tashkil qiladi.
Fizikadagi Mendeleyev tenglamasi

Bu tenglamani Klapeyron-Mendeleyev qonuni deb atash to’g’riroq va adolatliroq. Gap shundaki, u birinchi marta 1834 yilda frantsuz muhandisi Emil Klapeyron tomonidan qayd etilgan. U buni 19-asr boshlarida kashf etilgan Boyl-Mariott, Gey-Lyusak va Charlzning gaz qonunlarini tahlil qilish orqali amalga oshirdi.
Rossiyalik kimyogari Dmitriy Mendeleevning xizmatlari shundan iboratki, u tenglamaga zamonaviy va ishlatish uchun qulay matematik shaklni bergan. Xususan, Mendeleyev tenglamaga barcha gazlar uchun doimiy R=8, 314 J/(molK) kiritdi. Klapeyronning o‘zi hisoblash jarayonini qiyinlashtiradigan bir qancha empirik konstantalardan foydalangan.
Mendeleyev-Klapeyron tenglamasi quyidagicha yoziladi:
PV=nRT.
Bu tenglik ifodaning chap tomonidagi bosim P va hajm V koʻpaytmasi doimo absolyut harorat T va chap tomondagi n moddaning koʻpaytmasiga proportsional ekanligini bildiradi.
Oʻrganilayotgan ifoda toʻrtta parametrdan ikkitasini tuzatsangiz, istalgan gaz qonunini olish imkonini beradi. Izoprotsesslarda muhit bilan moddalar almashinuvi bo'lmagan yopiq tizimlar o'rganiladi (n=const). Bu jarayonlar yagona sobit termodinamik parametr (T, P yoki V) bilan tavsiflanadi.

Misol muammo
Endi Mendeleyev-Klapeyron tenglamasi bo’yicha masalani yechamiz. Ma'lumki, og'irligi 500 gramm bo'lgan kislorod 2 atmosfera bosimida 100 litr hajmli silindrda joylashgan. Tizim termodinamik muvozanatda ekanligini hisobga olsak, shardagi harorat qancha.
Eslatib o'tamiz, ta'rifga ko'ra, moddaning miqdori quyidagi formula bo'yicha hisoblanadi:
n=m/M.
Bu erda m - sistemaning barcha zarrachalarining massasi, M - ularning o'rtacha molyar massasi. Bu tenglik Mendeleyev tenglamasini quyidagi shaklda qayta yozishga imkon beradi:
PV=mRT/M.
Bu vazifa uchun ish formulasini qayerdan olamiz:
T=PVM/(mR).
Barcha miqdorlarni SI birliklariga aylantirish va ularni quyidagi ifodaga almashtirish qoladi:
T=21013250, 10, 032/(0, 58, 314)=156 K.
Hisoblangan harorat -117 oC. Bu haroratda kislorod hali ham gazsimon bo'lsa ham (u -182,96 oC da kondensatsiyalanadi), bunday sharoitda ideal gaz modelidan faqat hisoblangan qiymatning sifatli bahosini olish uchun foydalanish mumkin.






