Ideal gazning xossalarini o'rganish fizikaning muhim mavzusidir. Gaz tizimlarining xarakteristikalari bilan tanishish Boyl-Mariott tenglamasini ko'rib chiqishdan boshlanadi, chunki u ideal gazning birinchi eksperimental ravishda kashf etilgan qonunidir. Keling, buni maqolada batafsil ko'rib chiqaylik.
Ideal gaz deganda nima tushuniladi?
Boyl-Mariott qonuni va uni tavsiflovchi tenglama haqida gapirishdan oldin, keling, ideal gazni aniqlaymiz. Odatda uni tashkil etuvchi zarralar bir-biri bilan oʻzaro taʼsir qilmaydigan va oʻlchamlari zarralar orasidagi oʻrtacha masofaga nisbatan ahamiyatsiz darajada kichik boʻlgan suyuq modda sifatida tushuniladi.
Haqiqatdan ham har qanday gaz haqiqiydir, ya’ni uning tarkibidagi atom va molekulalar ma’lum hajmga ega bo’lib, Van der Vaals kuchlari yordamida bir-biri bilan o’zaro ta’sir qilmaydi. Biroq, yuqori mutlaq haroratlarda (300 K dan ortiq) va past bosimlarda (bir atmosferadan kam) atomlar va molekulalarning kinetik energiyasi Van der Vaals o'zaro ta'sirlari energiyasidan ancha yuqori bo'ladi, shuning uchun ko'rsatilgan haroratda haqiqiy gaz.yuqori aniqlikdagi shartlarni ideal deb hisoblash mumkin.
Boyl-Mariotte tenglamasi
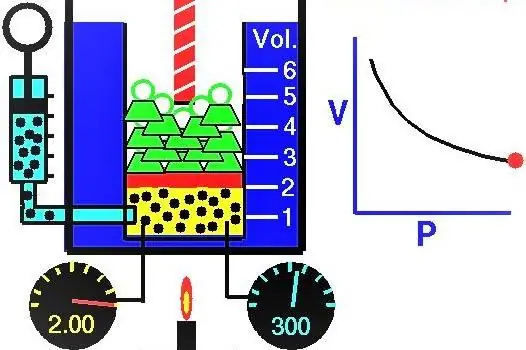
Gazlarning xossalari XVII-XIX asrlarda yevropalik olimlar faol ravishda tadqiq qilishgan. Eksperimental ravishda kashf etilgan birinchi gaz qonuni gaz tizimining kengayish va siqilish izotermik jarayonlarini tavsiflovchi qonun edi. Tegishli tajribalar 1662 yilda Robert Boyl va 1676 yilda Edm Mariotte tomonidan o'tkazildi. Bu olimlarning har biri mustaqil ravishda yopiq gaz tizimidagi izotermik jarayon davomida bosim hajmiga teskari o'zgarishini ko'rsatdi. Jarayonning eksperimental ravishda olingan matematik ifodasi quyidagi shaklda yoziladi:
PV=k
Bu erda P va V tizimdagi bosim va uning hajmi bo'lsa, k qandaydir doimiy bo'lib, uning qiymati gaz moddasi miqdori va uning haroratiga bog'liq. Agar siz P(V) funksiyaning grafikga bog‘liqligini qursangiz, u giperbola bo‘ladi. Quyida bu egri chiziqlarga misol keltirilgan.
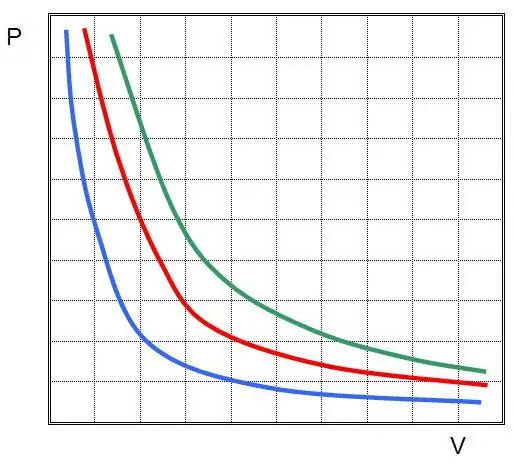
Yozma tenglik Boyl-Mario tenglamasi (qonun) deb ataladi. Ushbu qonunni qisqacha quyidagicha ifodalash mumkin: doimiy haroratda ideal gazning kengayishi undagi bosimning mutanosib pasayishiga olib keladi, aksincha, gaz tizimining izotermik siqilishi undagi bosimning mutanosib ortishi bilan birga keladi.
Ideal gaz tenglamasi
Boyl-Mariott qonuni Mendeleyev va nomi bilan atalgan umumiyroq qonunning alohida holatidir. Klapeyron. Emil Klapeyron 1834 yilda turli xil tashqi sharoitlarda gazlarning harakati haqidagi eksperimental ma'lumotlarni umumlashtirib, quyidagi tenglamani oldi:
PV=nRT
Boshqacha aytganda, gaz sistemasining V hajmining va undagi P bosimining mahsuloti absolyut harorat T va n moddaning miqdori ko’paytmasiga to’g’ri proporsionaldir. Bu mutanosiblik koeffitsienti R harfi bilan belgilanadi va gaz universal doimiysi deb ataladi. Yozma tenglamada R ning qiymati 1874 yilda Dmitriy Ivanovich Mendeleev tomonidan tuzilgan bir qator konstantalarni almashtirish hisobiga paydo bo'ldi.
Holatning universal tenglamasidan shuni koʻrish mumkinki, harorat va moddaning miqdori doimiyligi tenglamaning oʻng tomonining oʻzgarmasligini kafolatlaydi, yaʼni tenglamaning chap tomoni ham doimiy boʻlib qoladi.. Bu holda biz Boyl-Mariot tenglamasini olamiz.

Boshqa gaz qonunlari
Yuqoridagi paragrafda yozilgan Klapeyron-Mendeleyev tenglamasi uchta termodinamik parametrni o'z ichiga oladi: P, V va T. Agar ularning har biri o'zgarmas bo'lsa va qolgan ikkitasini o'zgartirishga ruxsat berilsa, Boyl-Mariottni olamiz, Charlz va Gey-Lyusak tenglamalari. Charlz qonuni izobarik jarayon uchun hajm va harorat o'rtasidagi to'g'ridan-to'g'ri proportsionallik haqida gapiradi va Gey-Lyussak qonuni izoxorik o'tishda gaz bosimi mutlaq haroratga to'g'ridan-to'g'ri proportsional ravishda ortadi yoki kamayadi. Tegishli tenglamalar quyidagicha ko'rinadi:
V/T=const qachon P=const;
P/T=const qachon V=const.
Shunday qilibShunday qilib, Boyl-Mariotte qonuni uchta asosiy gaz qonunlaridan biridir. Lekin u boshqalaridan grafik bogʻliqlik jihatidan farq qiladi: V(T) va P(T) funksiyalar toʻgʻri chiziq, P(V) funksiya giperbola.
Boyl-Mariott qonunini qoʻllash uchun topshiriq namunasi
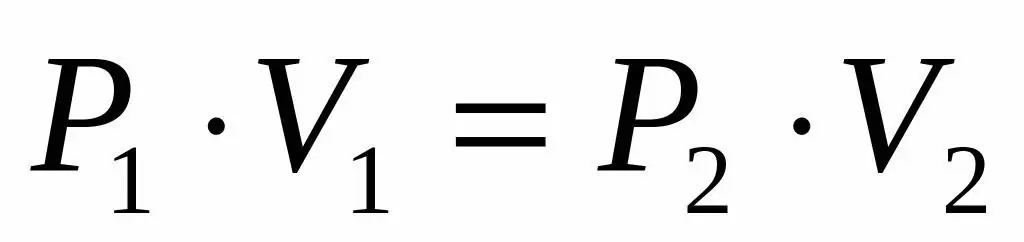
Boshlang'ich holatda piston ostidagi silindrdagi gaz hajmi 2 litr, bosimi esa 1 atmosfera edi. Piston ko'tarilgandan keyin gazning bosimi qanday edi va gaz tizimining hajmi 0,5 litrga oshdi. Jarayon izotermik hisoblanadi.
Bizga ideal gazning bosimi va hajmi berilganligi va uning kengayishi davomida harorat oʻzgarmasligini ham bilganimiz uchun Boyl-Mariot tenglamasidan quyidagi koʻrinishda foydalanishimiz mumkin:
P1V1=P2V 2
Bu tenglik ma'lum haroratdagi gazning har bir holati uchun hajm-bosim mahsuloti doimiy ekanligini bildiradi. Tenglikdan P2 qiymatini ifodalab, biz yakuniy formulani olamiz:
P2=P1V1/V 2
Bosimni hisoblashda siz bu holda tizimdan tashqari birliklardan foydalanishingiz mumkin, chunki litrlar qisqaradi va biz atmosferalarda P2 bosimini olamiz. Shart ma'lumotlarini almashtirib, biz muammoning savoliga javobga erishamiz: P2=0,8 atmosfera.






