Termodinamikaning muhim boʻlimi moddaning turli fazalari orasidagi oʻzgarishlarni oʻrganishdir, chunki bu jarayonlar amalda sodir boʻladi va maʼlum sharoitlarda tizimning harakatini bashorat qilish uchun fundamental ahamiyatga ega. Ushbu o'zgarishlar fazali o'tishlar deb ataladi va maqola ularga bag'ishlangan.
Faza va tizim komponenti tushunchasi

Fizikada fazaviy oʻtishlarni koʻrib chiqishga oʻtishdan oldin fazaning oʻzi tushunchasini aniqlash zarur. Umumiy fizika kursidan ma'lumki, moddaning uchta holati mavjud: gazsimon, qattiq va suyuq. Ilm-fanning maxsus bo'limida - termodinamikada - qonunlar materiyaning fazalari uchun tuzilgan, lekin ularning yig'ilish holatlari uchun emas. Faza deganda bir jinsli tuzilishga ega boʻlgan, oʻziga xos fizik-kimyoviy xossalari bilan ajralib turadigan va materiyaning qolgan qismidan chegaralar bilan ajratilgan, interfaza deb ataladigan maʼlum hajmdagi moddalar tushuniladi.
Shunday qilib, "faza" tushunchasi xususiyatlar haqida amaliy jihatdan muhimroq ma'lumotlarni o'z ichiga oladi.materiya uning yig'ilish holatidan ko'ra. Masalan, temir kabi metallning qattiq holati quyidagi fazalarda bo'lishi mumkin: past haroratli magnit tana markazlashtirilgan kub (BCC), past haroratli magnit bo'lmagan bcc, yuz markazlashtirilgan kub (fcc) va yuqori - harorat magnit bo'lmagan bcc.
Termodinamika qonunlarida "faza" tushunchasidan tashqari "komponentlar" atamasi ham qo'llaniladi, ya'ni muayyan tizimni tashkil etuvchi kimyoviy elementlar sonini bildiradi. Bu shuni anglatadiki, faza monokomponent (1 kimyoviy element) yoki ko'p komponentli (bir nechta kimyoviy element) bo'lishi mumkin.
Gibbs teoremasi va tizim fazalari orasidagi muvozanat

Fazalar almashinuvini tushunish uchun ular orasidagi muvozanat sharoitlarini bilish kerak. Bu shartlarni matematik tarzda ularning har biri uchun Gibbs tenglamalari tizimini yechish orqali olish mumkin, bunda tizimning tashqi ta’sirdan ajratilgan umumiy Gibbs energiyasi o‘zgarishni to‘xtatganda muvozanat holatiga erishiladi.
Ko'rsatilgan tenglamalar tizimini echish natijasida bir necha fazalar o'rtasida muvozanat mavjudligi uchun shartlar olinadi: izolyatsiyalangan tizim faqat bosimlar, har bir komponentning kimyoviy potentsiallari va barcha fazalardagi haroratlar bo'lganda rivojlanishni to'xtatadi. bir-biriga teng.
Muvozanat uchun Gibbs faza qoidasi

Bir necha faza va komponentlardan tashkil topgan tizim nafaqat muvozanatda boʻlishi mumkinmuayyan sharoitlarda, masalan, ma'lum bir harorat va bosimda. Muvozanat uchun Gibbs teoremasining ba'zi o'zgaruvchilari fazalar sonini va ushbu muvozanatdagi komponentlar sonini saqlab qolgan holda o'zgartirilishi mumkin. Tizimdagi muvozanatni buzmasdan o'zgartirilishi mumkin bo'lgan o'zgaruvchilar soni ushbu tizimning erkinliklari soni deb ataladi.
F faza va k komponentdan tashkil topgan tizimning l erkinliklari soni Gibbs faza qoidasidan yagona aniqlanadi. Bu qoida matematik tarzda quyidagicha yoziladi: l + f=k + 2. Bu qoida bilan qanday ishlash kerak? Juda onson. Masalan, sistema f=3 muvozanat fazasidan iborat ekanligi ma’lum. Bunday tizimda eng kam komponentlar soni qancha bo'lishi mumkin? Savolga quyidagicha mulohaza yuritish orqali javob berishingiz mumkin: muvozanat holatida eng qattiq shartlar faqat ma'lum ko'rsatkichlarda amalga oshirilganda mavjud bo'ladi, ya'ni har qanday termodinamik parametrning o'zgarishi muvozanatga olib keladi. Bu erkinliklar soni l=0 ekanligini bildiradi. l va f ning ma'lum qiymatlarini almashtirib, biz k=1 ni olamiz, ya'ni uchta faza muvozanatda bo'lgan tizim bitta komponentdan iborat bo'lishi mumkin. Bunga eng yaxshi misol suvning uchlik nuqtasi bo'lib, u erda muz, suyuq suv va bug' ma'lum harorat va bosimlarda muvozanatda bo'ladi.
Fazali oʻzgarishlar tasnifi
Muvozanat holatidagi tizimdagi ba'zi termodinamik parametrlarni o'zgartirishni boshlasangiz, bir faza qanday yo'qolib, ikkinchisi paydo bo'lishini kuzatishingiz mumkin. Bu jarayonning oddiy misoli muzning qizdirilganda erishi.
Gibbs tenglamasi faqat ikkita o'zgaruvchiga (bosim va harorat) bog'liqligini va fazaviy o'tish bu o'zgaruvchilarning o'zgarishini o'z ichiga olishini hisobga olsak, matematik tarzda fazalar orasidagi o'tishni Gibbs energiyasini uning o'ziga nisbatan farqlash orqali tasvirlash mumkin. o'zgaruvchilar. Aynan shu yondashuvni avstriyalik fizik Pol Erenfest 1933 yilda fazalar muvozanatining o'zgarishi bilan sodir bo'ladigan barcha ma'lum termodinamik jarayonlarning tasnifini tuzganida qo'llagan.
Termodinamikaning asoslaridan kelib chiqadiki, Gibbs energiyasining haroratga nisbatan birinchi hosilasi sistema entropiyasining oʻzgarishiga teng. Gibbs energiyasining bosimga nisbatan hosilasi hajmning o'zgarishiga teng. Agar tizimdagi fazalar o'zgarganda, entropiya yoki hajm tanaffusga uchrasa, ya'ni ular keskin o'zgarsa, ular birinchi tartibli fazali o'tish haqida gapiradi.
Bundan tashqari, harorat va bosimga nisbatan Gibbs energiyasining ikkinchi hosilalari mos ravishda issiqlik sig'imi va hajmli kengayish koeffitsientidir. Agar fazalar orasidagi o'zgarish ko'rsatilgan jismoniy miqdorlarning qiymatlaridagi uzilish bilan birga bo'lsa, ikkinchi tartibli fazali o'tish haqida gapiriladi.
Fazalar orasidagi oʻzgarishlarga misollar

Tabiatda juda ko'p turli xil o'tishlar mavjud. Ushbu tasnif doirasida birinchi turdagi o'tishlarning yorqin misollari tizimda hajmning sakrashi sodir bo'lganda, metallarning erishi yoki havodan suv bug'ining kondensatsiyasi jarayonlaridir.
Agar biz ikkinchi tartibli oʻtishlar haqida gapiradigan boʻlsak, unda yorqin misollar temirning magnitdan paramagnit holatga oʻtishini haroratda keltirish mumkin.768 ºC yoki mutlaq nolga yaqin haroratlarda metall o'tkazgichning o'ta o'tkazuvchanlik holatiga aylanishi.
Birinchi turdagi oʻtishlarni tavsiflovchi tenglamalar
Amalda koʻpincha tizimda fazali oʻzgarishlar sodir boʻlganda harorat, bosim va yutilgan (boʻshatilgan) energiya qanday oʻzgarishini bilish zarur. Buning uchun ikkita muhim tenglama qo'llaniladi. Ular termodinamika asoslarini bilish asosida olinadi:
- Klapeyron formulasi, u turli fazalar orasidagi oʻzgarishlar paytida bosim va harorat oʻrtasidagi bogʻliqlikni oʻrnatadi.
- Transformatsiya jarayonida soʻrilgan (boʻshatilgan) energiya va tizim haroratini bogʻlovchi Klauzius formulasi.
Har ikkala tenglamadan foydalanish nafaqat fizik kattaliklarning miqdoriy bog’liqliklarini olishda, balki faza diagrammalarida muvozanat egri chizig’ining qiyaligi belgisini aniqlashda hamdir.
Ikkinchi turdagi oʻtishlarni tavsiflash uchun tenglama

1-va 2-turdagi fazali oʻtishlar turli tenglamalar bilan tavsiflanadi, chunki ikkinchi tartibli oʻtishlar uchun Klauzius va Klauzius tenglamalarini qoʻllash matematik noaniqlikka olib keladi.
Oxirgisini tavsiflash uchun issiqlik sig'imi va transformatsiya jarayonida hajmli kengayish koeffitsienti o'zgarishini bilish orqali bosim va harorat o'zgarishi o'rtasidagi munosabatni o'rnatadigan Erenfest tenglamalari qo'llaniladi. Erenfest tenglamalari magnit maydon bo'lmaganda Supero'tkazuvchilar va Supero'tkazuvchilar o'tishlarini tasvirlash uchun ishlatiladi.
Ahamiyatfaza diagrammasi
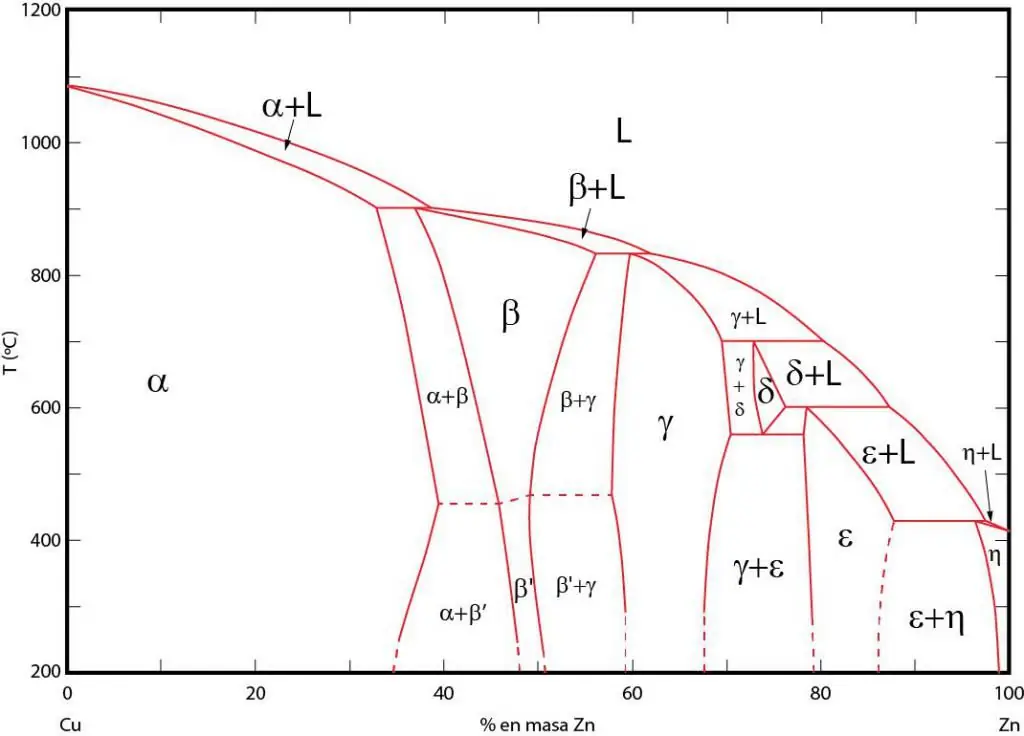
Faza diagrammalari mos keladigan fazalar muvozanatda boʻlgan maydonlarning grafik tasviridir. Bu maydonlar fazalar orasidagi muvozanat chiziqlari bilan ajratilgan. Ko'pincha P-T (bosim-harorat), T-V (harorat-hajm) va P-V (bosim-hajm) faza diagrammalaridan foydalaniladi.
Faza diagrammalarining ahamiyati shundan iboratki, ular tashqi sharoitlar mos ravishda oʻzgarganda tizimning qaysi fazada boʻlishini bashorat qilish imkonini beradi. Ushbu ma'lumot istalgan xususiyatlarga ega strukturani olish uchun turli materiallarni issiqlik bilan ishlov berishda qo'llaniladi.






