Biz yashayotgan dunyo tasavvur qilib boʻlmaydigan darajada goʻzal va hayot yoʻnalishini belgilab beruvchi turli jarayonlarga toʻla. Bu jarayonlarning barchasini tanish fan - fizika o'rganadi. Bu koinotning kelib chiqishi haqida hech bo'lmaganda bir oz tasavvurga ega bo'lish imkoniyatini beradi. Ushbu maqolada biz molekulyar kinetik nazariya, uning tenglamalari, turlari va formulalari kabi tushunchani ko'rib chiqamiz. Biroq, bu masalalarni chuqurroq o'rganishga o'tishdan oldin, siz o'zingiz uchun fizikaning ma'nosini va u o'rganadigan sohalarni aniqlab olishingiz kerak.
Fizika nima?

Aslida, bu juda keng qamrovli fan va, ehtimol, insoniyat tarixidagi eng fundamental fanlardan biridir. Misol uchun, agar xuddi shu informatika inson faoliyatining deyarli barcha sohalari bilan bog'liq bo'lsa, u hisoblash dizayni yoki multfilmlar yaratish bo'ladimi, u holda fizika hayotning o'zi, uning murakkab jarayonlari va oqimlarining tavsifidir. Keling, uning ma'nosini iloji boricha soddalashtirib, tushunishga harakat qilaylik.
Shunday qilibShunday qilib, fizika energiya va materiyani, ular orasidagi bog'lanishlarni o'rganish, ulkan olamimizda sodir bo'layotgan ko'plab jarayonlarni tushuntirish bilan shug'ullanadigan fandir. Moddalar tuzilishining molekulyar-kinetik nazariyasi fizika nazariyalari va sohalari dengizidagi kichik bir tomchidir.
Bu fan batafsil oʻrganadigan energiya turli shakllarda ifodalanishi mumkin. Masalan, yorug'lik, harakat, tortishish, radiatsiya, elektr va boshqa ko'plab shakllarda. Biz ushbu maqolada ushbu shakllar tuzilishining molekulyar kinetik nazariyasiga to'xtalib o'tamiz.
Materiyani o'rganish bizga materiyaning atom tuzilishi haqida tushuncha beradi. Aytgancha, u molekulyar-kinetik nazariyadan kelib chiqadi. Materiyaning tuzilishi haqidagi fan bizning mavjudligimizning ma'nosini, hayotning paydo bo'lish sabablarini va olamning o'zini tushunishga va topishga imkon beradi. Keling, moddaning molekulyar-kinetik nazariyasini o'rganishga harakat qilaylik.
Birinchidan, terminologiya va har qanday xulosani toʻliq tushunish uchun biroz kirish kerak.
Fizika mavzulari
Molekulyar-kinetik nazariya nima degan savolga javob berib, fizikaning bo'limlari haqida gapirmasdan bo'lmaydi. Ularning har biri inson hayotining ma'lum bir sohasini batafsil o'rganish va tushuntirish bilan shug'ullanadi. Ular quyidagicha tasniflanadi:
- Mexanika, u yana ikkita boʻlimga boʻlingan: kinematika va dinamika.
- Statik.
- Termodinamika.
- Molekulyar qism.
- Elektrodinamika.
- Optika.
- Kvantlar fizikasi va atom yadrosi.
Keling, molekulyar haqida alohida gaplashaylikfizika, chunki u molekulyar-kinetik nazariyaga asoslanadi.
Termodinamika nima?
Umuman olganda, molekulyar qism va termodinamika bir-biri bilan chambarchas bog'liq bo'lgan fizikaning bo'limlari bo'lib, ular faqat fizik tizimlarning umumiy sonining makroskopik komponentini o'rganadi. Shuni esda tutish kerakki, bu fanlar jismlar va moddalarning ichki holatini aniq tasvirlaydi. Masalan, ularning isitish, kristallanish, bug'lanish va kondensatsiya paytidagi holati, atom darajasida. Boshqacha qilib aytadigan bo'lsak, molekulyar fizika - bu juda ko'p sonli zarralar: atomlar va molekulalardan tashkil topgan tizimlar haqidagi fan.
Mana shu fanlar molekulyar kinetik nazariyaning asosiy qoidalarini oʻrgangan.
Biz yettinchi sinfda ham mikro va makroolam, tizim tushunchalari bilan tanishdik. Ushbu atamalarni xotirada yangilash ortiqcha bo'lmaydi.
Mikrodunyo, uning nomidan ham ko’rishimiz mumkinki, elementar zarrachalardan tashkil topgan. Boshqacha qilib aytganda, bu kichik zarralar dunyosi. Ularning o'lchamlari 10-18 m dan 10-4 m gacha bo'lgan oraliqda o'lchanadi va ularning haqiqiy holati cheksiz va cheksiz bo'lishi mumkin. nomutanosib kichik intervallar, masalan, 10-20 s.
Macroworld koʻplab elementar zarrachalardan tashkil topgan barqaror shakldagi jismlar va tizimlarni koʻrib chiqadi. Bunday tizimlar inson o‘lchamimizga mos keladi.
Bundan tashqari, mega dunyo degan narsa bor. U ulkan sayyoralar, kosmik galaktikalar va komplekslardan tashkil topgan.
Asosiynazariya
Endi biz fizikaning asosiy atamalarini qisqacha takrorlab, eslab qoldik, toʻgʻridan-toʻgʻri ushbu maqolaning asosiy mavzusiga oʻtishimiz mumkin.
Molekulyar-kinetik nazariya birinchi marta XIX asrda paydo bo'lgan va shakllantirilgan. Uning mohiyati shundaki, u Robert Guk, Isaak kabi taniqli olimlarning taxminlaridan to'plangan uchta asosiy qoidaga asoslanib, har qanday moddaning tuzilishini (ko'pincha qattiq va suyuq jismlarga qaraganda gazlarning tuzilishini) batafsil tavsiflaydi. Nyuton, Daniel Bernulli, Mixail Lomonosov va boshqalar.
Molekulyar kinetik nazariyaning asosiy qoidalari quyidagicha eshitiladi:
- Mutlaqo barcha moddalar (suyuq, qattiq yoki gazsimon bo'lishidan qat'iy nazar) murakkab tuzilishga ega bo'lib, ular kichikroq zarrachalar: molekulalar va atomlardan iborat. Atomlar ba'zan "elementar molekulalar" deb ataladi.
- Bu elementar zarralarning barchasi doimo uzluksiz va xaotik harakat holatidadir. Har birimiz ushbu taklifning to'g'ridan-to'g'ri isbotiga duch keldik, lekin, ehtimol, unga unchalik ahamiyat bermadik. Misol uchun, barchamiz quyosh nurlari fonida chang zarralari doimo tartibsiz yo'nalishda harakat qilishini ko'rdik. Buning sababi, atomlarning bir-birlari bilan o'zaro itarilishi, doimiy ravishda bir-biriga kinetik energiya berib turishi. Bu hodisa birinchi marta 1827 yilda o'rganilgan va u kashfiyotchi sharafiga nomlangan - "Braun harakati".
- Barcha elementar zarralar bir-biri bilan uzluksiz ta'sir qilish jarayonida.elektr jinsiga ega bo'lgan ba'zi kuchlar.
Ta'kidlash joizki, ikkinchi pozitsiyani tavsiflovchi yana bir misol, masalan, gazlarning molekulyar kinetik nazariyasiga ham tegishli bo'lishi mumkin bo'lgan diffuziya. Biz buni kundalik hayotda, bir nechta sinov va nazoratlarda uchratamiz, shuning uchun bu haqda tasavvurga ega bo‘lish juda muhim.
Avval quyidagi misollarni koʻrib chiqing:
Doktor tasodifan stol ustidagi kolbadagi spirtni to'kib yubordi. Yoki atir shishangizni tushirib yuborgandirsiz va u butun polga tarqalib ketgandir.
Nima uchun bu ikki holatda alkogol hidi ham, parfyum hidi ham ma'lum vaqtdan so'ng bu moddalarning tarkibi to'kilgan joyni emas, balki butun xonani to'ldiradi?
Javob oddiy: diffuziya.
Diffuziya - bu nima? U qanday oqadi?

Bu ma'lum bir moddani (odatda gaz) tashkil etuvchi zarralar boshqasining molekulalararo bo'shliqlariga kirib borishi jarayonidir. Yuqoridagi misollarimizda quyidagilar sodir bo'ldi: termal, ya'ni uzluksiz va dissotsiatsiyalangan harakat tufayli alkogol va / yoki parfyum molekulalari havo molekulalari orasidagi bo'shliqlarga tushib ketdi. Asta-sekin, atomlar va havo molekulalari bilan to'qnashuv ta'sirida ular xona bo'ylab tarqaldi. Aytgancha, diffuziyaning intensivligi, ya'ni uning oqimining tezligi diffuziyada ishtirok etuvchi moddalarning zichligiga, shuningdek, kinetik deb ataladigan ularning atomlari va molekulalarining harakat energiyasiga bog'liq. Kinetik energiya qanchalik katta bo'lsa, bu molekulalarning tezligi va intensivligi shunchalik yuqori bo'ladi.
Eng tez diffuziya jarayonini gazlardagi diffuziya deb atash mumkin. Buning sababi shundaki, gaz o'z tarkibida bir hil emas, ya'ni gazlardagi molekulalararo bo'shliqlar mos ravishda katta hajmdagi joyni egallaydi va ularga begona moddaning atomlari va molekulalarini olish jarayoni osonroq va tezroq ketadi..
Suyuqlikda bu jarayon biroz sekinroq. Bir krujka choyda shakar kublarining erishi qattiq moddaning suyuqlikdagi tarqalishiga misoldir.
Lekin eng uzoq vaqt qattiq kristall tuzilishga ega jismlarda diffuziya hisoblanadi. Bu aynan shunday, chunki qattiq jismlarning tuzilishi bir hil va kuchli kristall panjaraga ega bo'lib, uning hujayralarida qattiq jismning atomlari tebranadi. Misol uchun, agar ikkita metall panjaraning sirtlari yaxshilab tozalanib, keyin bir-biriga tegib qo'yilsa, etarlicha uzoq vaqt o'tgach, biz bir metallning boshqasida va aksincha, bo'laklarini aniqlay olamiz.
Boshqa fundamental boʻlimlar kabi fizikaning asosiy nazariyasi ham alohida qismlarga boʻlinadi: tasnif, turlar, formulalar, tenglamalar va hokazo. Shunday qilib, biz molekulyar kinetik nazariyaning asoslarini o'rgandik. Bu siz alohida nazariy bloklarni ko'rib chiqishga bemalol o'tishingiz mumkinligini anglatadi.
Gazlarning molekulyar-kinetik nazariyasi
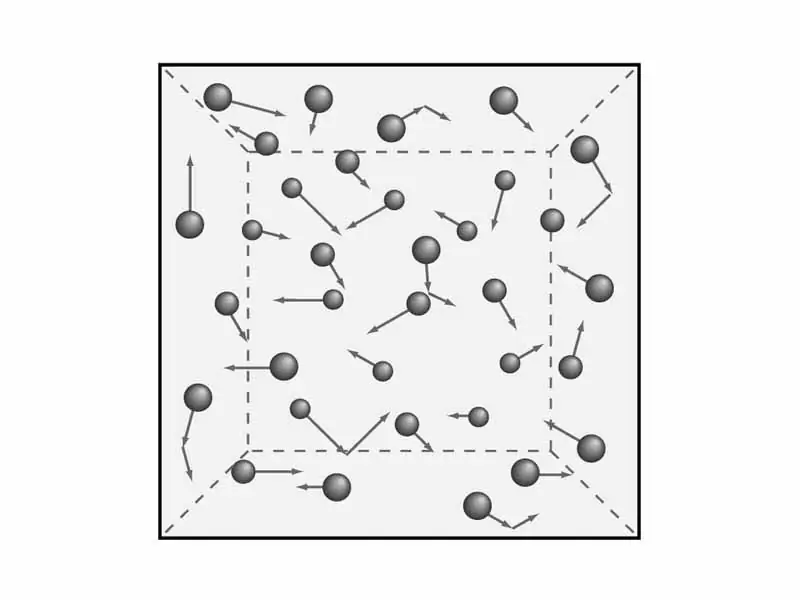
Gaz nazariyasi qoidalarini tushunish kerak. Yuqorida aytib o'tganimizdek, biz gazlarning bosim va harorat kabi makroskopik xususiyatlarini ko'rib chiqamiz. Bugazlarning molekulyar-kinetik nazariyasi tenglamasini olish uchun keyinroq kerak bo'ladi. Ammo matematika - keyinroq, endi esa nazariya va shunga mos ravishda fizika bilan shug'ullanamiz.
Olimlar gazlarning kinetik modelini tushunishga xizmat qiluvchi gazlarning molekulyar nazariyasining beshta qoidasini ishlab chiqdilar. Ular shunday eshitiladi:
- Barcha gazlar ma'lum bir o'lchamga ega bo'lmagan, ammo ma'lum bir massaga ega bo'lgan elementar zarralardan iborat. Boshqacha qilib aytganda, bu zarrachalarning hajmi ular orasidagi uzunlikka nisbatan minimaldir.
- Gazlarning atomlari va molekulalari amalda potentsial energiyaga ega emas, mos ravishda qonunga koʻra, barcha energiya kinetikga teng.
- Biz bu pozitsiya bilan avvalroq tanishgan edik - Broun harakati. Ya'ni, gaz zarralari doimo uzluksiz va tartibsiz harakatda bo'ladi.
- Tezlik va energiya xabari bilan birga keladigan gaz zarralarining mutlaqo barcha oʻzaro toʻqnashuvlari toʻliq elastikdir. Bu shuni anglatadiki, to‘qnashuv paytida ularning kinetik energiyasida energiya yo‘qolmaydi yoki keskin sakrashlar bo‘lmaydi.
- Oddiy sharoitda va doimiy haroratda deyarli barcha gazlarning zarracha harakatining oʻrtacha energiyasi bir xil boʻladi.
Biz gazlarning molekulyar-kinetik nazariyasining ushbu turdagi tenglamalari orqali beshinchi pozitsiyani qayta yozishimiz mumkin:
E=1/2mv^2=3/2kT, bu yerda k - Boltsman doimiysi; T - Kelvindagi harorat.
Bu tenglama bizga gazning elementar zarrachalarining tezligi va ularning mutlaq harorati oʻrtasidagi bogʻliqlikni tushunishga yordam beradi. Shunga ko'ra, ularning mutlaq darajasi qanchalik balandharorat, ularning tezligi va kinetik energiyasi shunchalik katta bo'ladi.
Gaz bosimi
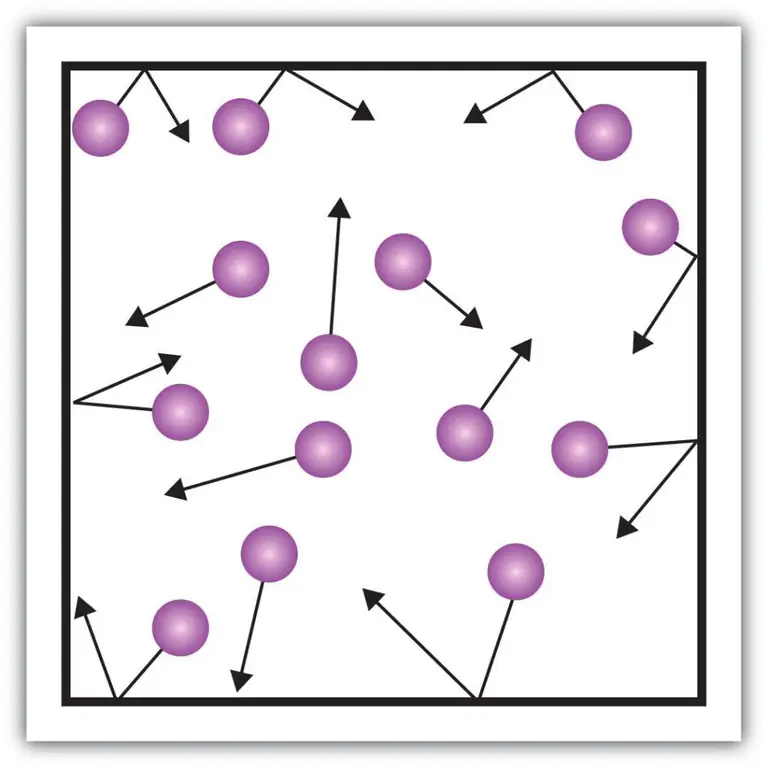
Gazlar bosimi kabi xarakteristikaning bunday makroskopik komponentlarini kinetik nazariya yordamida ham tushuntirish mumkin. Buning uchun quyidagi misolni tasavvur qilaylik.
Faraz qilaylik, qandaydir gaz molekulasi uzunligi L bo’lgan qutichada bo’lsin. Yuqorida bayon qilingan gaz nazariyasi qoidalaridan foydalanamiz va molekulyar sfera faqat x bo’ylab harakatlanishini hisobga olamiz. -o'q. Shunday qilib, biz tomir devorlaridan biri (quti) bilan elastik to'qnashuv jarayonini kuzatishimiz mumkin bo'ladi.
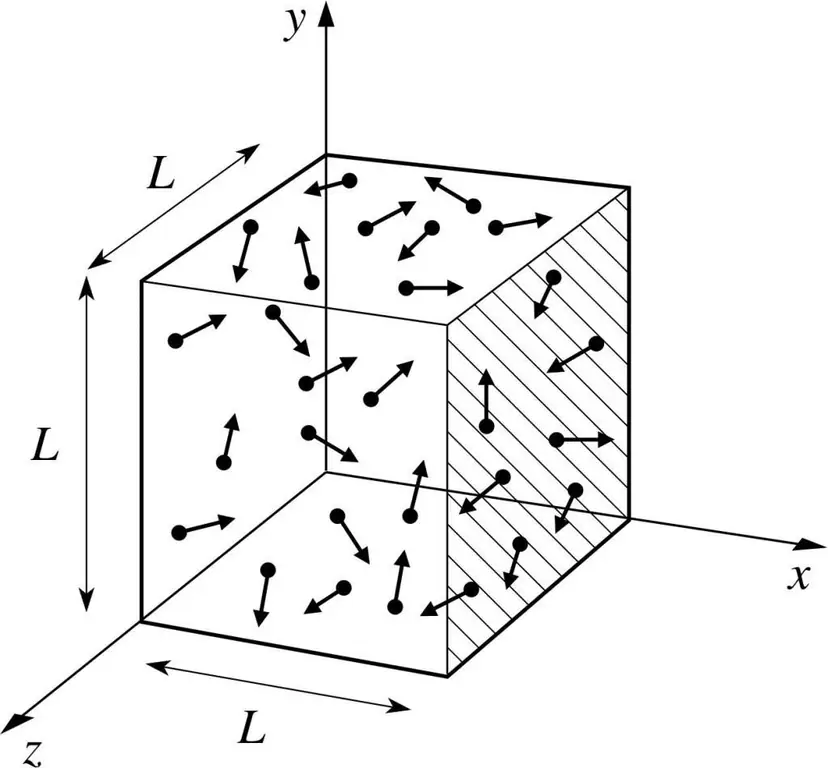
Davom etayotgan toʻqnashuvning impulsi, biz bilganimizdek, quyidagi formula bilan aniqlanadi: p=mv, lekin bu holda bu formula proyeksiya koʻrinishini oladi: p=mv(x).
Biz faqat x o'qining o'lchamini, ya'ni x o'qini ko'rib chiqayotganimiz uchun impulsning umumiy o'zgarishi formula bilan ifodalanadi: mv(x) - m(-v() x))=2mv(x).
Keyin, Nyutonning ikkinchi qonuni yordamida ob'ektimiz ta'sir qiladigan kuchni ko'rib chiqing: F=ma=P/t.
Bu formulalardan gaz tarafidagi bosimni ifodalaymiz: P=F/a;
Endi hosil boʻlgan formulaga kuch ifodasini almashtiramiz va quyidagini olamiz: P=mv(x)^2/L^3.
Shundan so'ng bizning tayyor bosim formulamiz gaz molekulalarining N-soni uchun yozilishi mumkin. Boshqacha qilib aytganda, u shunday ko'rinadi:
P=Nmv(x)^2/V, bu yerda v tezlik va V ovoz balandligi.
Endi gaz bosimi boʻyicha bir nechta asosiy qoidalarni ajratib koʻrsatishga harakat qilaylik:
- Bu orqali oʻzini namoyon qiladimolekulalarning u joylashgan ob'ekt devorlarining molekulalari bilan to'qnashuvi.
- Bosimning kattaligi molekulalarning tomir devorlariga ta'sir qilish kuchi va tezligiga to'g'ridan-to'g'ri proportsionaldir.
Nazariya bo'yicha ba'zi qisqacha xulosalar
Molekulyar kinetik nazariyaning asosiy tenglamasini koʻrib chiqishdan oldin yuqoridagi fikrlar va nazariyalardan bir nechta qisqacha xulosalarni taqdim etamiz:
- Atom va molekulalarining oʻrtacha harakat energiyasining oʻlchovi mutlaq haroratdir.
- Ikki turli gazlar bir xil haroratda boʻlsa, ularning molekulalari bir xil oʻrtacha kinetik energiyaga ega boʻladi.
- Gaz zarralarining energiyasi oʻrtacha kvadrat tezligiga toʻgʻridan-toʻgʻri proportsional: E=1/2mv^2.
- Gaz molekulalari mos ravishda oʻrtacha kinetik energiyaga va oʻrtacha tezlikka ega boʻlsa-da, alohida zarralar har xil tezlikda harakat qiladi: baʼzilari tez, baʼzilari sekin.
- Harorat qancha yuqori boʻlsa, molekulalarning tezligi shunchalik yuqori boʻladi.
- Gazning haroratini necha marta oshirsak (masalan, ikki barobar), uning zarrachalarining harakat energiyasi shuncha marta ortadi (mos ravishda ikki barobar ortadi).
Asosiy tenglama va formulalar

Molekulyar-kinetik nazariyaning asosiy tenglamasi mikrodunyoning miqdorlari va shunga mos ravishda makroskopik, ya'ni o'lchangan miqdorlar o'rtasidagi munosabatni o'rnatishga imkon beradi.
Molekulyar nazariya koʻrib chiqishi mumkin boʻlgan eng oddiy modellardan biri ideal gaz modelidir.
Shuni aytishingiz mumkinbu ideal gazning molekulyar kinetik nazariyasi tomonidan o'rganiladigan xayoliy modelning bir turi bo'lib, unda:
- eng oddiy gaz zarralari bir-biri bilan ham, har qanday tomir devorlarining molekulalari bilan ham o'zaro ta'sir qiluvchi mukammal elastik sharlar deb hisoblanadi, faqat bitta holatda - mutlaqo elastik to'qnashuv;
- gaz ichidagi tortishish kuchlari yo'q yoki ularni e'tiborsiz qoldirish mumkin;
- Gazning ichki strukturasi elementlarini moddiy nuqtalar sifatida olish mumkin, ya'ni ularning hajmini ham e'tiborsiz qoldirish mumkin.
Bunday modelni hisobga olgan holda nemis asli fizik Rudolf Klauzius mikro- va makroskopik parametrlar munosabati orqali gaz bosimi formulasini yozdi. Bu shunday ko'rinadi:
p=1/3m(0)nv^2.
Keyinchalik bu formula ideal gazning molekulyar-kinetik nazariyasining asosiy tenglamasi deb ataladi. U bir necha xil shakllarda taqdim etilishi mumkin. Endi bizning vazifamiz molekulyar fizika, molekulyar kinetik nazariya kabi bo'limlarni va shuning uchun ularning to'liq tenglamalari va turlarini ko'rsatishdir. Shuning uchun, asosiy formulaning boshqa variantlarini ko'rib chiqish mantiqan to'g'ri keladi.
Biz bilamizki, gaz molekulalarining harakatini tavsiflovchi oʻrtacha energiyani quyidagi formula yordamida topish mumkin: E=m(0)v^2/2.
Bunday holatda biz dastlabki bosim formulasidagi m(0)v^2 ifodasini oʻrtacha kinetik energiya bilan almashtira olamiz. Buning natijasida gazlarning molekulyar kinetik nazariyasining asosiy tenglamasini quyidagi ko'rinishda tuzish imkoniyatiga ega bo'lamiz: p=2/3nE.
Bundan tashqari, barchamiz bilamizki, m(0)n ifodasini ikkita qismning koʻpaytmasi sifatida yozish mumkin:
m/NN/V=m/V=r.
Ushbu manipulyatsiyalardan so'ng biz ideal gazning molekulyar-kinetik nazariyasi tenglamasi formulasini uchinchi, boshqacha ko'rinishda qayta yozishimiz mumkin:
p=1/3rv^2.
Xo'sh, bu mavzu bo'yicha bilishingiz kerak bo'lgan narsa shudir. Olingan bilimlarni qisqacha (va unchalik emas) xulosalar shaklida tizimlashtirishgina qoladi.
"Molekulyar-kinetik nazariya" mavzusidagi barcha umumiy xulosalar va formulalar
Keling, boshlaymiz.
Birinchi:
Fizika tabiiy fanlar kursiga kiritilgan fundamental fan boʻlib, u modda va energiyaning xossalarini, ularning tuzilishini, noorganik tabiat qonuniyatlarini oʻrganadi.
U quyidagi boʻlimlarni oʻz ichiga oladi:
- mexanika (kinematika va dinamika);
- statik;
- termodinamik;
- elektrodinamika;
- molekulyar kesim;
- optika;
- kvantlar fizikasi va atom yadrosi.
Ikkinchi:
Zarralar fizikasi va termodinamika bir-biri bilan chambarchas bog'liq bo'lgan sohalar bo'lib, ular umumiy jismoniy tizimlar sonining faqat makroskopik komponentini, ya'ni juda ko'p elementar zarrachalardan tashkil topgan tizimlarni o'rganadi.
Ular molekulyar kinetik nazariyaga asoslanadi.
Uchinchisi:
Maslaning mohiyati shu. Molekulyar kinetik nazariya moddaning tuzilishini (ko'pincha qattiq moddalarga qaraganda gazlarning tuzilishini) batafsil tavsiflaydi.va suyuq jismlar), taniqli olimlarning taxminlaridan to'plangan uchta asosiy taxminlarga asoslanadi. Ular orasida: Robert Guk, Isaak Nyuton, Daniel Bernulli, Mixail Lomonosov va boshqalar.
Toʻrtinchisi:
Molekulyar kinetik nazariyaning uchta asosiy qoidasi:
- Barcha moddalar (suyuq, qattiq yoki gazsimon bo'lishidan qat'iy nazar) kichikroq zarralar: molekulalar va atomlardan iborat murakkab tuzilishga ega.
- Bu oddiy zarralarning barchasi uzluksiz xaotik harakatda. Misol: Braun harakati va diffuziya.
- Barcha molekulalar har qanday sharoitda bir-biri bilan elektr togʻ jinsiga ega boʻlgan maʼlum kuchlar bilan taʼsir oʻtkazadi.
Molekulyar-kinetik nazariyaning ushbu qoidalarining har biri materiya tuzilishini oʻrganishda mustahkam asosdir.
Beshinchisi:
Gaz modeli uchun molekulyar nazariyaning bir nechta asosiy nuqtalari:
- Barcha gazlar ma'lum bir o'lchamga ega bo'lmagan, ammo ma'lum bir massaga ega bo'lgan elementar zarralardan iborat. Boshqacha qilib aytganda, bu zarrachalarning hajmi ular orasidagi masofalarga nisbatan minimaldir.
- Gazlarning atomlari va molekulalari amalda potentsial energiyaga ega emas, mos ravishda ularning umumiy energiyasi kinetik energiyaga teng.
- Biz bu pozitsiya bilan avvalroq tanishgan edik - Broun harakati. Ya'ni, gaz zarralari doimo uzluksiz va tasodifiy harakatda bo'ladi.
- Tezlik va energiya xabari bilan birga gazlar atomlari va molekulalarining mutlaqo barcha oʻzaro toʻqnashuvlari toʻliq elastikdir. Buto‘qnashuv vaqtida ularning kinetik energiyasida energiya yo‘qolmasligi yoki keskin sakrashlar bo‘lmasligini bildiradi.
- Oddiy sharoitda va doimiy haroratda deyarli barcha gazlarning oʻrtacha kinetik energiyasi bir xil boʻladi.
Oltinchisi:
Gazlar haqidagi nazariyadan xulosalar:
- Mutlaq harorat uning atomlari va molekulalarining oʻrtacha kinetik energiyasining oʻlchovidir.
- Ikki turli gazlar bir xil haroratda boʻlsa, ularning molekulalari bir xil oʻrtacha kinetik energiyaga ega boʻladi.
- Gaz zarralarining o'rtacha kinetik energiyasi o'rtacha kvadrat tezligiga to'g'ridan-to'g'ri proportsionaldir: E=1/2mv^2.
- Gaz molekulalari mos ravishda oʻrtacha kinetik energiyaga va oʻrtacha tezlikka ega boʻlsa-da, alohida zarralar har xil tezlikda harakat qiladi: baʼzilari tez, baʼzilari sekin.
- Harorat qancha yuqori boʻlsa, molekulalarning tezligi shunchalik yuqori boʻladi.
- Gazning haroratini necha marta oshirsak (masalan, ikki baravar), uning zarrachalarining o'rtacha kinetik energiyasi ham shuncha marta ortadi (mos ravishda ikki barobar ortadi).
- Gazning u joylashgan idish devorlariga bosimi va molekulalarning bu devorlarga ta'sir qilish intensivligi o'rtasidagi bog'liqlik to'g'ridan-to'g'ri proportsionaldir: ta'sir qancha ko'p bo'lsa, bosim shunchalik yuqori bo'ladi va aksincha..
Yettinchisi:
Ideal gaz modeli - bu quyidagi shartlar bajarilishi kerak bo'lgan model:
- Gaz molekulalari mukammal elastik sharlar boʻlishi mumkin va shunday hisoblanadi.
- Bu toʻplar bir-biri bilan va istalganining devorlari bilan oʻzaro taʼsir qilishi mumkinkema faqat bitta holatda - mutlaqo elastik to'qnashuv.
- Gazning atomlari va molekulalari orasidagi oʻzaro taʼsirni tavsiflovchi kuchlar mavjud emas yoki ularni eʼtiborsiz qoldirish mumkin.
- Atomlar va molekulalar moddiy nuqtalar sifatida qaraladi, ya'ni ularning hajmini ham e'tiborsiz qoldirish mumkin.
Sakkizinchi:
Barcha asosiy tenglamalarni beramiz va "Molekulyar-kinetik nazariya" mavzusidagi formulalarni ko'rsatamiz:
p=1/3m(0)nv^2 - nemis fizigi Rudolf Klauzius tomonidan olingan ideal gaz modeli uchun asosiy tenglama.
p=2/3nE - ideal gazning molekulyar-kinetik nazariyasining asosiy tenglamasi. Molekulalarning oʻrtacha kinetik energiyasidan olingan.
r=1/3rv^2 - bir xil tenglama, lekin ideal gaz molekulalarining zichligi va ildiz oʻrtacha kvadrat tezligi orqali koʻrib chiqiladi.
m(0)=M/N(a) - Avogadro raqami orqali bitta molekulaning massasini topish formulasi.
v^2=(v(1)+v(2)+v(3)+…)/N - molekulalarning oʻrtacha kvadrat tezligini topish formulasi, bu yerda v(1), v(2), v (3) va boshqalar - birinchi molekula tezligi, ikkinchi, uchinchi va boshqalar n-molekulagacha.
n=N/V - molekulalarning konsentratsiyasini topish formulasi, bu erda N - gaz hajmidagi molekulalar soni V ma'lum hajmgacha.
E=mv^2/2=3/2kT - molekulalarning o'rtacha kinetik energiyasini topish formulalari, bu erda v^2 - molekulalarning o'rtacha kvadrat tezligi, k - doimiy. avstriyalik Lyudvig Boltsman fizikasi nomi bilan atalgan qiymat, T esa gazning harorati.
p=nkT - konsentratsiya bo'yicha bosim formulasi, doimiyBoltsman va mutlaq harorat T. Undan rus olimi Mendeleyev va fransuz fizik-muhandis Klayperon tomonidan kashf etilgan yana bir fundamental formula kelib chiqadi:
pV=m/MRT, bu yerda R=kN(a) gazlar uchun universal doimiydir.
Endi turli izo-jarayonlar uchun konstantalarni ko'rsatamiz: izobar, izoxorik, izotermik va adiabatik.
pV/T=const - gazning massasi va tarkibi doimiy bo'lganda bajariladi.
rV=const - harorat ham doimiy bo'lsa.
V/T=const - agar gaz bosimi doimiy bo'lsa.
p/T=const - ovoz balandligi doimiy bo'lsa.
Ehtimol, bu mavzu boʻyicha bilishingiz kerak boʻlgan narsa shudir.
Bugun biz nazariy fizika, uning koʻplab boʻlimlari va bloklari kabi ilmiy sohaga kirdik. Batafsilroq, biz fizikaning fundamental molekulyar fizika va termodinamika, yaʼni molekulyar-kinetik nazariya kabi sohasiga toʻxtalib oʻtdik, bu esa dastlabki oʻrganishda hech qanday qiyinchilik tugʻdirmaydi, lekin aslida koʻplab tuzoqlarga ega.. Bu ideal gaz modeli haqidagi tushunchamizni kengaytiradi, biz ham batafsil o'rganib chiqdik. Bundan tashqari, shuni ta'kidlash joizki, biz molekulyar nazariyaning asosiy tenglamalari bilan ularning turli xil o'zgarishlari bilan tanishdik, shuningdek, ushbu mavzu bo'yicha ma'lum noma'lum miqdorlarni topish uchun barcha eng kerakli formulalarni ko'rib chiqdik. Bu, ayniqsa, yozishga tayyorgarlik ko'rayotganda foydali bo'ladi. har qanday testlar, imtihonlar va testlar yoki fizika haqidagi umumiy dunyoqarash va bilimlarni kengaytirish uchun.
Ushbu maqola siz uchun foydali boʻldi deb umid qilamiz va siz undan molekulyar kinetik nazariyaning asosiy qoidalari kabi termodinamika ustunlari boʻyicha bilimlaringizni mustahkamlab, faqat eng kerakli maʼlumotlarni oldingiz.






